


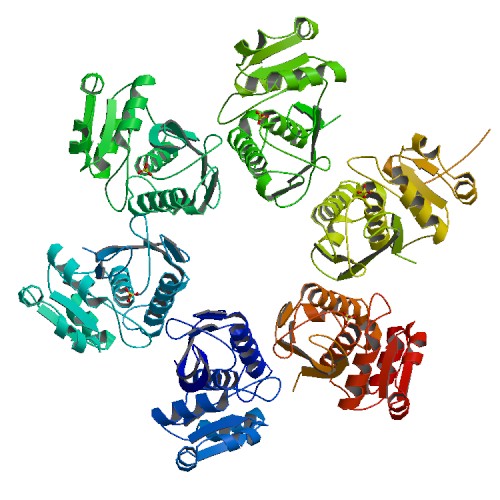
 Первый домен (зеленый) - это АТФ-зависимая протеаза La (LON), которая отвечает
за связь с субстратом. Второй домен (красный) - AAA или AAA + (является аббревиатурой для
АТФазы, связанной с различной клеточной деятельностью). Третий домен (синий) - С-концевой
протеолитический домен Lon протеазы (S16)
[6].
Более подробное описание доменов представлено в Таблице 1.
Первый домен (зеленый) - это АТФ-зависимая протеаза La (LON), которая отвечает
за связь с субстратом. Второй домен (красный) - AAA или AAA + (является аббревиатурой для
АТФазы, связанной с различной клеточной деятельностью). Третий домен (синий) - С-концевой
протеолитический домен Lon протеазы (S16)
[6].
Более подробное описание доменов представлено в Таблице 1.
| Таблица 1. Доменная архитектура белка P0A9M0 | |||
| Домен | Структура | Описание | Пример структуры |
| ATP-dependent protease La (LON) substrate-binding domain (АТФ-зависимая протеаза La (LON) субстрат-связывающего домена) |  |
АТФ-зависимые Lon - протеазы сохраняется во всех живых организмах и катализируют быстрый оборот короткоживущих регуляторных белков и многих поврежденных или денатурированных белков. В молекулярной биологии семейство Lon-протеазы представлено протеазами. Это N-концевой домен, который можно найти у архей, бактерий и эукариот . Lon-протеазы являются АТФ-зависимыми сериновыми пептидазами, принадлежащими к Merops-пептидазам семейства S16 (на рисунке слева - Кристаллическая структура N-концевого домена E.Coli Lon протеазы). [7]. | Crystal structure of N-terminal domain of E.Coli Lon Protease (Кристаллическая структура
N-концевого домена E.Coli Lon - протеиназы)  |
| ATPase family associated with various cellular activities (AAA) (Семейство АТФазы, связанное с различной клеточной деятельностью (AAA)) |  |
Это большое, функционально разнообразное белковое семейство, принадлежащее к AAA надсемейству кольцеобразной Р-петли NTPases, которое проявляет свою активность через зависящую от энергии ремоделирования или транслокации макромолекулу. Члены семьи AAA найдены во всех организмах, они имеют важное значение для многих клеточных функций. Также участвует в таких процессах, как репликация ДНК, деградации белка, слияние мембран, микротрубочек, разрыв пероксиса биогенез, сигнальная трансдукция и регуляция экспрессии генов (на рисунке слева - N-этилмалеимид-чувствительный фактор). [8]. | TRIGONAL CRYSTAL FORM OF HEAT SHOCK LOCUS U (HSLU) FROM ESCHERICHIA COLI (Тригональная
кристаллическая форма теплового шока LOCUS U (HSLU) ОТ кишечной палочки) 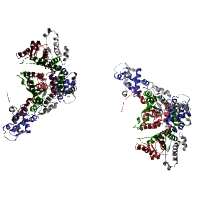 |
| Lon protease (S16) C-terminal proteolytic domain (С-концевой протолитический домен Lon протеазы (S16)) |  |
Серинпротеазы Lon должны гидролизовать АТФ для деградирования белковых субстратов. В кишечной палочке эти протеазы участвуют в обороте внутриклеточных белков, в том числе аномальных белков после теплового шока. В Lon протеазы классифицируются как семья S16 в Merops.(на рисунке слева - Кристаллическая структура N-концевого домена E.Coli Lon протеазы). [9]. | The Lon-like protease MtaLonC in complex with lactacystin (Lon-протеаза, как MtaLonC в
комплексе с lactacystin) 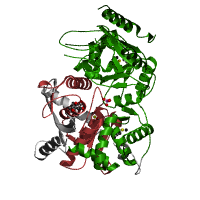 |
Дальнейший поиск я произвожу по домену (ААА).

 Первый домен (зеленый) - это домен MIT (микротрубочковое взаимодействие и транспорт). Второй (красный)
- уже описываемый AAA или AAA +. Третий домен (синий) - Vps4 C-концевой домен олигомеризации. Подробное
описание ранее не упоминаемых доменов можно увидеть в Таблице 2.
Первый домен (зеленый) - это домен MIT (микротрубочковое взаимодействие и транспорт). Второй (красный)
- уже описываемый AAA или AAA +. Третий домен (синий) - Vps4 C-концевой домен олигомеризации. Подробное
описание ранее не упоминаемых доменов можно увидеть в Таблице 2.
| Таблица 2. Доменная архитектура белка P52917 | |||
| Домен | Структура | Описание | Пример структуры |
| MIT (microtubule interacting and transport) (MIT (микротрубочковое взаимодействие и транспорт)) | - | Домен MIT образует пучок из трех ассимитиричных спиралей и связывает ESCRT-III (эндосая сортировка комплексов, необходимых для транспортировки) [11]. | VPS4B MIT-CHMP2B Complex (VPS4B MIT-CHMP2B комплекс)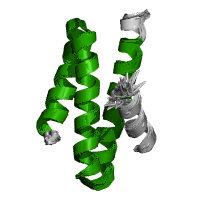
|
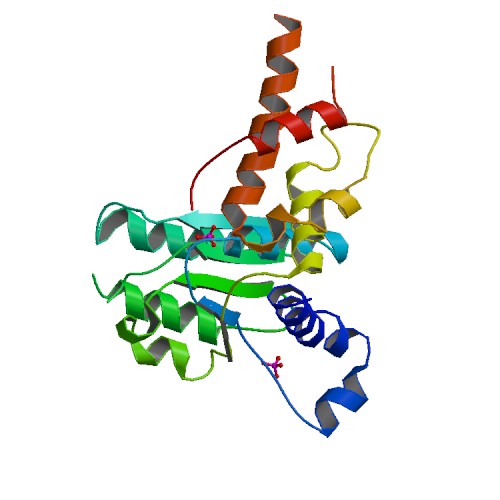
| Vps4 C terminal oligomerisation domain (Vps4 C-концевой домен олигомеризации) | - | Этот домен находится в терминале C АТФазы белков , участвующих в сортировке вакуоли. Он образует структуру альфа - спирали и необходим для олигомеризации [12]. | Crystal structure of mouse SKD1/VPS4B apo-form (Кристаллическая структура мышиного SKD1 /
VPS4B апо-формы)  |
 Первый домен (зеленый) - это нуклеолин-связывающий домен. Второй и третий домены (красные)
- это уже описываемый AAA или AAA +. Подробное описание ранее не упоминаемых доменов можно увидеть
в Таблице 3.
Первый домен (зеленый) - это нуклеолин-связывающий домен. Второй и третий домены (красные)
- это уже описываемый AAA или AAA +. Подробное описание ранее не упоминаемых доменов можно увидеть
в Таблице 3.
| Таблица 3. Доменная архитектура белка O15381 | |||
| Домен | Структура | Описание | Пример структуры |
| Nucleolin binding domain (Нуклеолин-связывающий домен) | - | Этот домен принимает вид трех спиралей, напоминающих часть крыла. Он связывает нуклеолин [14]. | Structure and function of the N-terminal nucleolin binding domain of nuclear valocine
containing protein like 2 (NVL2) harboring a nucleolar localization signal (Структура и функция
N-концевого нуклеолин связывающего домена ядерного valocine, содержащиая такие белки, как 2
(NVL2) укрывающие ядрышки сигналы локализации) 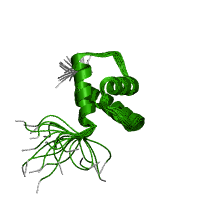 |
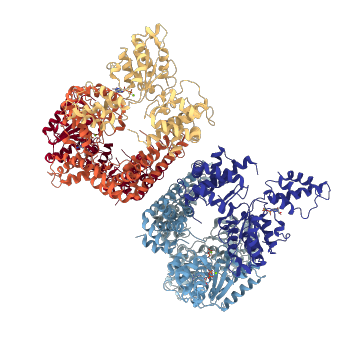
 Первый домен (зеленый) - FTSH внеклеточная. Второй домен (красный) - это уже описываемый AAA
или AAA +. Третий домен (синий) принадлежит к семье пептидазы M41. Подробное описание ранее не
упоминаемых доменов можно увидеть в Таблице 4.
Первый домен (зеленый) - FTSH внеклеточная. Второй домен (красный) - это уже описываемый AAA
или AAA +. Третий домен (синий) принадлежит к семье пептидазы M41. Подробное описание ранее не
упоминаемых доменов можно увидеть в Таблице 4.
| Таблица 4. Доменная архитектура белка Q9WZ49 | |||
| Домен | Структура | Описание | Пример структуры |
| FtsH Extracellular (FTSH внеклеточная) | - | Этот домен находится в семье FTSH белков. FTSH является единственной мембраносвязанной АТФ-зависимой протеазой повсеместно сохраняющейся у прокариот. Некоторые признаки указывают на то, что она является одним из основных механизмов самозащиты прокариот, который проверяет, правильно ли белки сложены (личные набл: Йейтс C). Точная функция этой N-концевой области остается неясной [16]. | Escherichia coli FtsH hexameric N-domain (FTSH гексамерный N-домен кишечной палочки)
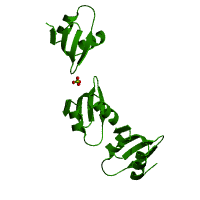 |
| Peptidase family M41 (семья Пептидазы M41) | - | В этих ферментах присутствует двухвалентный катион, как правило, цинк, но может быть кобальт, марганец или медь, который активирует молекулу воды. Пептидазы семьи М41 принадлежат к большей семье металлопротеаз цинка. Это семейство включает в себя белок деления клеток FTSH и дрожжи митохондриальных цепных комплексов сборки, а также дыхательный белок, который представляет собой предполагаемую АТФ-зависимую протеазу, необходимую для сборки митохондриальной дыхательной цепи и АТФазных комплексов. [17]. | Truncated FtsH from A. aeolicus (Усе FTSH от А. aeolicus)
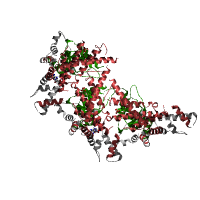 |
© Serebrennikova Maria 2017